从针尖到舌尖的逆袭,口服多肽药物成新宠
2024-12-05
11月中旬,强生和Protagonist共同宣布,Icotrokinra(JNJ-2113,前称PN-235)的关键3期研究取得了积极的顶线结果。该3期研究在第16周达到了银屑病面积和严重程度指数(PASI)90和研究者整体评估(IGA)的共同主要终点0/1反应,并且反应率在第24周继续改善。
JNJ-2113是第一个选择性阻断IL-23受体的靶向口服肽,适用于12岁及以上患有中度至重度斑块状银屑病(PsO)的成人和青少年。

口服多肽药物:多重优势助力多肽药物蓬勃发展
1、多肽药物兼具小分子化药及蛋白类药物优点
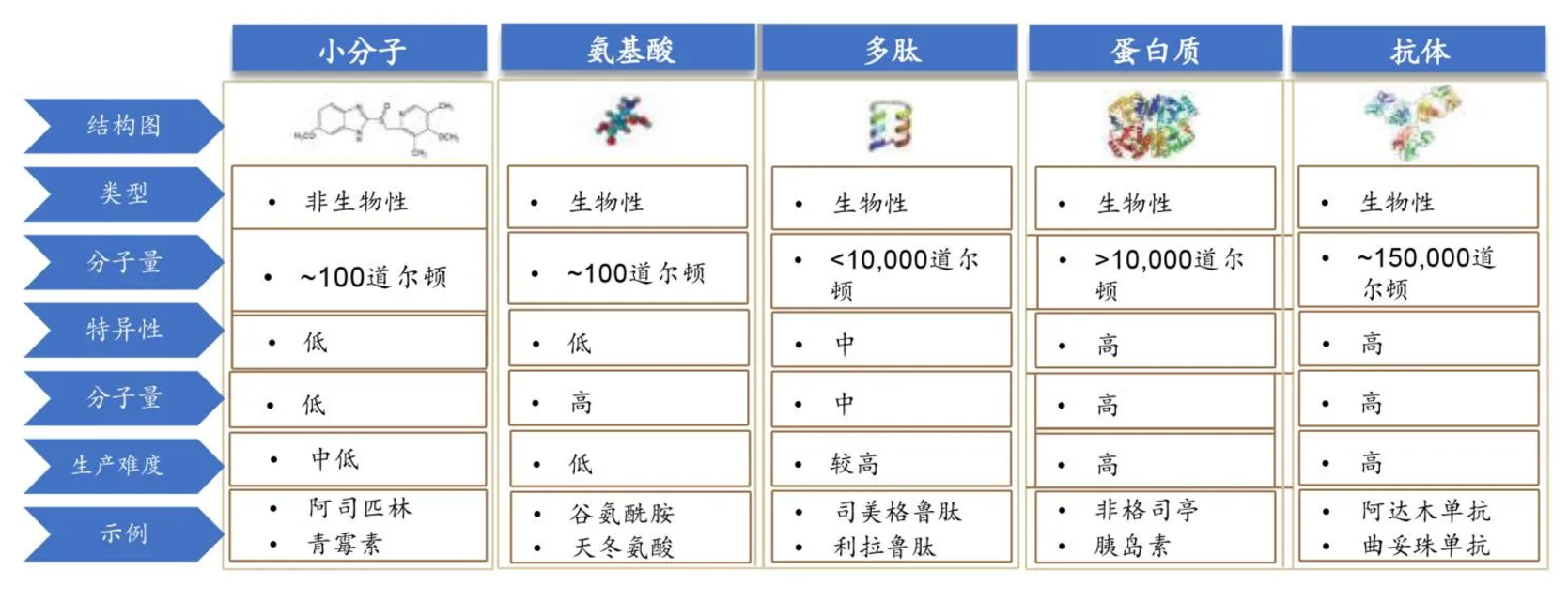
多肽:包含10-100个氨基酸,分子大小介于小分子化药(MW<500)和蛋白药物(MW>10000)之间。
与蛋白质药物相比:多肽具有空间结构较简单、稳定性较高、免疫原性低等优势,同时兼具蛋白质类药物特异性强、疗效好的特点。
与小分子化药相比:多肽药物在生物活性、特异性以及解决复杂疾病方面更优,同时具有小分子药物质量可控、结构易确证的特点。多肽药物在生产制备和临床应用中由于其高活性、低剂量、低毒性、质量可控的优势,适用于解决小分子化学药难以解决的复杂疾病。
2、多肽药物市场规模巨大,应用集中于肿瘤、消化道等领域
自1902年首个多肽物质在人体内被发现,多肽研究至今已发展超过百年。1922年多肽(胰岛素)首次应用于人体,开启了多肽药物波澜壮阔的新篇章,1963年多肽固相合成技术(SPPS)的发明为多肽药物带来了里程碑式的革命,其合成方便,迅速,成为多肽合成的主要方法,催生了多肽药物的快速发展。70年代以后,人工合成多肽开始陆续运用于临床。目前全球获批的多肽类药物约180种,根据肽研社统计,2021年全球多肽药物(包含胰岛素)TOP32销售额达505.3亿美元,市场规模巨大。市场格局看,在获批多肽药物中,抗肿瘤领域数量最多(30%),其次消化道领域(14%)、糖尿病领域(13%)和罕见病(11%)。
3、口服多肽的研发成为新热点
自2000年以来,天然多肽不断得到丰富,特别是来自毒液的多肽组学和新的化学修饰方法的推动,促进了新型多肽药物的发现。多功能肽、约束肽、偶联肽、口服肽、长效化、递送系统等新兴技术的出现极大地推动了多肽药物领域的繁荣发展,并催生了更加前沿的“多肽新经济产业”。
然而多肽类药物渗透性差、易被胃肠道中的蛋白酶降解,因此上市的多肽类药物多为注射剂。尽管注射剂市场强劲,但其对患者有侵入性,影响患者依从性,约60%的糖尿病患者因无法忍受长期重复的注射给药而不能实现稳定的血糖控制。此外,注射剂增加了制造和储存的复杂性,最终影响医疗成本。因此,口服多肽药物的研发一直是研究热点,但成功转化的不多,主要因为口服多肽药物的吸收面临重重困难。
多肽类药物的口服遭遇重重“研发瓶颈”
1、口服多肽药物开发挑战
(1)首先,与普遍存在的“多肽不能被口服”的认知不同,饮食中的蛋白质在体内被降解后,形成多肽片段,小于11个氨基酸片段的多肽可以被胃肠道吸收。同理,经过碱基加工的11个氨基酸以下片段的多肽可以被胃肠道吸收,但临床中使用的多肽类药物的分子量很少为11个氨基酸以下的序列,例如胰岛素、GLP-1RA都是几十个氨基酸,不满足能够口服的要求。
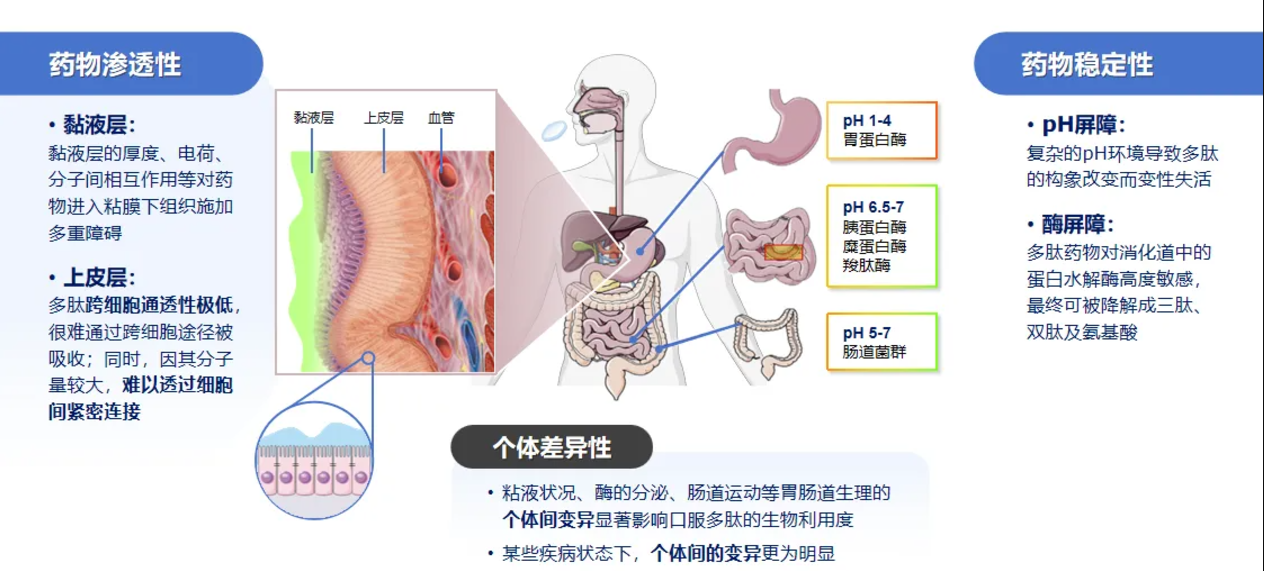
(2)其次,多肽有两个方面的不稳定。
遇酸不稳定:pH值降低,肽键可能被水解,造成肽链不稳定。
遇酶不稳定:人体消化道中存在很多酶类,最经典的是胃蛋白酶,还包括胰腺分泌的氨基肽酶及其他蛋白酶,可将多肽进一步水解成小片段,失去药物的生物学活性。很多多肽类药物在口服过程中被胃酸、胃蛋白酶、其他氨基肽酶所水解,水解后的片段失去药物疗效。
(3)最后,多肽类药物的吸收个体差异较大。由于不同患者在性别、年龄、胃肠道功能、饮食习惯、服药与用餐关系等方面存在差异,这些均可导致药物吸收的巨大差异。·
口服大分子吸收的最大障碍是通过肠上皮细胞,这通常是利用细胞旁路或跨细胞通路实现的。研究人员已经对此开发了各种新策略,来解决大分子口服生物利用度差的问题。这些措施包括防止胃肠道降解的策略,例如酶抑制剂、封装成纳米粒子、脂质体和微球,以及增加肠道通透性的策略,比如使用渗透促进剂,以及大分子的化学修饰(例如lipidation)以增强与白蛋白的结合,提高半衰期并促进大分子在肠上皮细胞中的摄取。
2、提高多肽口服吸收的策略
多肽药物想要达到理想的口服吸收,往往需要多维度的助力。
结构优化:针对多肽链的结构修饰,防止多肽在胃肠道水解,提高多肽的胃肠道稳定性;提高多肽的体内代谢稳定性,延长生物半衰期。
促渗透剂:通过促渗透剂改变胃肠道上皮的紧密连接,提高渗透性,也是目前口服多肽的常用策略。常见的促渗透剂包括表面活性剂癸酸钠、辛酸钠,螯合剂EDTA、柠檬酸等。
制剂手段:比如自乳化制剂,通过提高难溶性药物在胃肠道的溶解度,促进吸收;肠溶胶囊可避免多肽药物在胃部释放,减少胃内降解等。
pH调节剂:胃肠道的酶活性与pH值息息相关,pH调节剂可通过改变胃肠道局部的pH值,影响酶的活性,减少多肽在胃肠道的降解。
口服多肽研发进展
1、打破了多肽胃肠道吸收的壁垒,口服多肽药物不断上市
随着对多肽口服吸收机理的深入了解,科学家开发的技术手段打破了多肽胃肠道吸收的壁垒,一些口服多肽药物已经成功上市。
环孢菌素为分子量1202.61的环肽,是第一个上市的口服多肽药物。但是环孢菌素本身的分子量较小,环肽的结构也增加了稳定性。环孢菌素上市之后多年,口服多肽药物一直没有取得显著性进展。
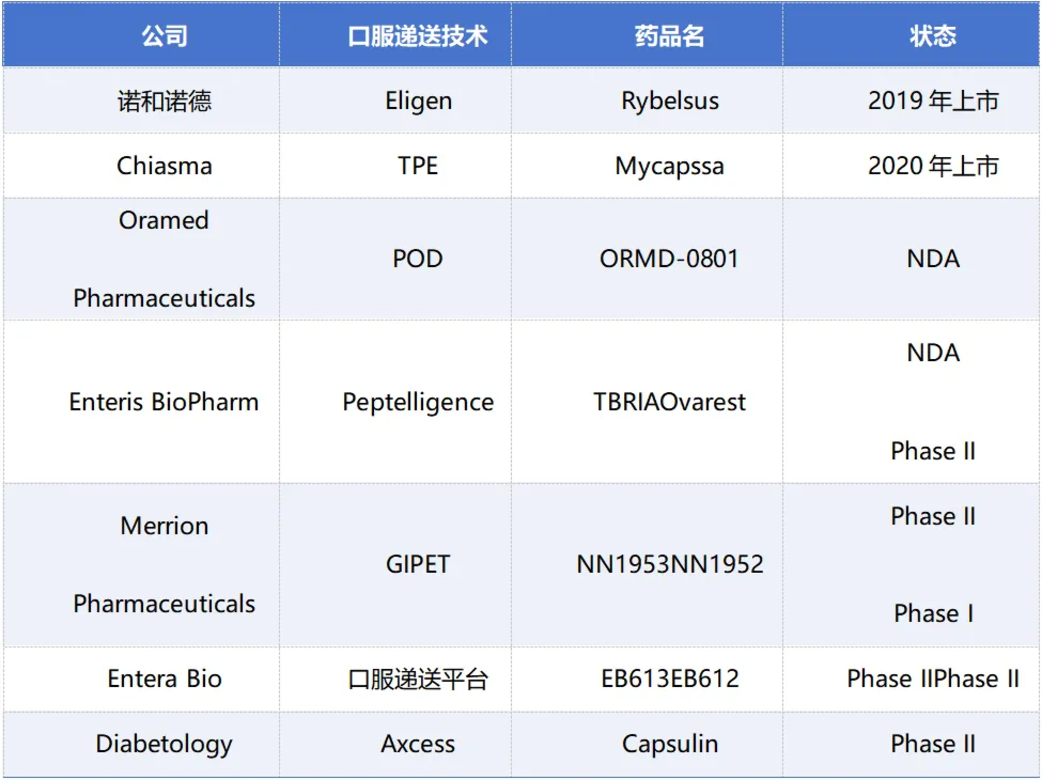
直到2019年9月,诺和诺德的II型糖尿病药物,GLP-1多肽semaglutide(Rybelsus®)以口服制剂的形式获批上市,成为继cyclosporin A(环孢素A,Neoral®)、Desmopressin(去氨加压素,DDAVP®)后的又一款实现口服递送的多肽药物。Semaglutide在口服给药后能够保持很长的半衰期(约153-160小时,而注射后为168小时)。Rybelsus®的成功,除了18碳二羧酸的脂化修饰之外,渗透促进剂SNAC(8-(2-羟基苯甲酰胺基)辛酸钠)的作用至关重要。
2、GLP-1受体激动剂(GLP-1RA)类药物
代谢性疾病作为慢性病,口服制剂是重要的研发方向。
GLP-1受体激动剂是多肽类药物,主流用药方法是皮下注射。相对于注射剂型,口服药可以增加患者使用便捷性与用药依从性,也可以消除部分患者对于注射剂的恐惧。然而口服容易被胃液以及胃肠道中的各种酶降解,生物利用度低,因此口服而不被降解的GLP-1类药物是研发的新热点。但是全球具备研发出GLP-1RA口服小分子的医药公司寥寥无几。借助“SNAC吸收促进剂”创新技术,司美格鲁肽片成功突破了技术壁垒,实现了GLP-1RA类药物经口服途径给药的历史性跨越,成为第一个真正意义上的口服多肽类药物。
伴随着口服多肽递送技术的不断迭代更新,希望后续有更多口服多肽进入临床。
3、JNJ-2113:全球首款口服IL-23R多肽拮抗剂
11月18日,强生(J&J)与Protagonist Therapeutics公布了其口服IL-23R靶向拮抗多肽icotrokinra(JNJ-2113)用于斑块状银屑病的的两项关键的三期临床研究取得了积极的初步结果。JNJ-2113是一种竞争性多肽拮抗剂,能与IL-23R高亲和力的结合,对人类T细胞中的IL-23信号具有强效的选择性抑制作用,由强生和Protagonist Therapeutics共同开发,是首个旨在阻断IL-23R的在研靶向口服多肽。Icotrokinra是首款选择性阻断IL-23受体的靶向口服肽类药物,用于治疗12岁及以上患有中重度斑块状银屑病(PsO)的患者。Icotrokinra能够以个位数的皮摩尔亲和力与IL-23R结合,并对人类T细胞中的IL-23信号转导产生强效的选择性抑制作用。2017年,强生与Protagonist Therapeutics达成近10亿美元的合作协议,共同开发针对IL-23R的口服疗法。
4、目前口服多肽药物项目研究情况
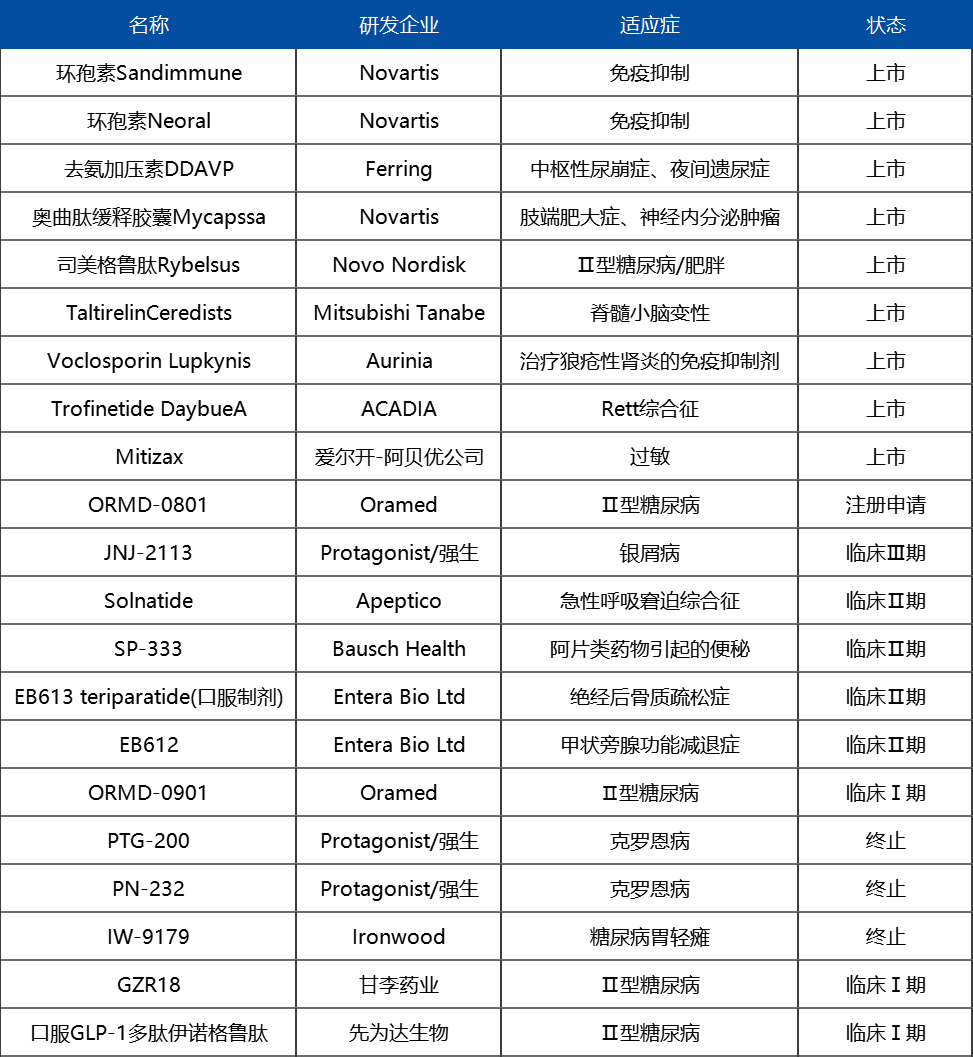
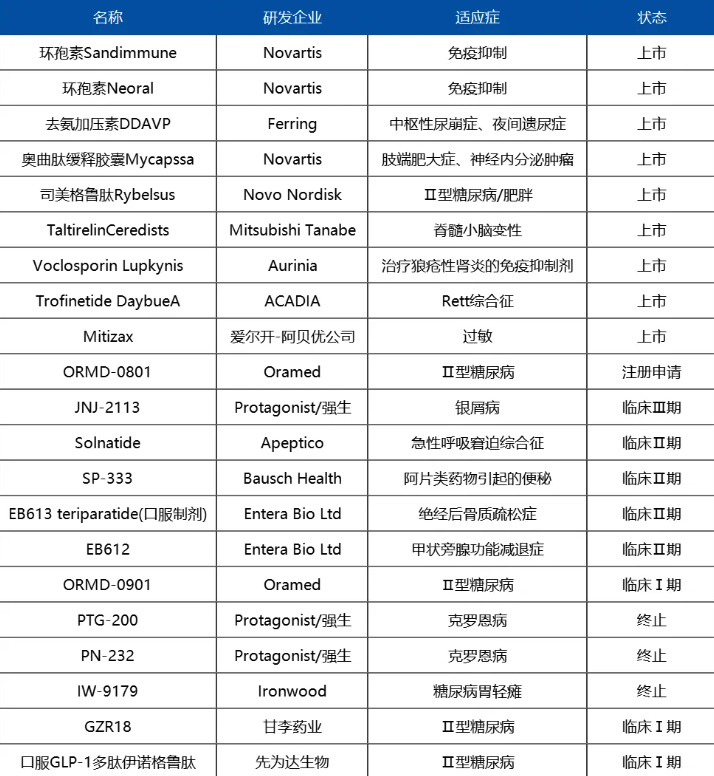
总结之下,针对多肽类药品的口服研发需从其本身性质出发进行优化,确保药物在低剂量即可发挥治疗效果,同时具备胃肠道稳定性,拥有较长的半衰期和宽广的治疗窗,这是开发此类药品的基础。此外,剂型设计也至关重要,包括释放动力学和肠溶性包衣以实现靶向递送,这都可能提升口服肽的生物利用率。然而,对于固态剂型溶解影响口服多肽在胃肠道特定部位的吸收机制我们仍有许多未知。
展望
由于胃肠道生理环境,多肽类药物易发生降解,且不易吸收,种种障碍导致口服多肽的生物利用度极低,因此多肽药物往往是注射给药。但对于糖尿病、免疫性疾病等需要长期用药患者来说,长期注射的痛感和心理负担不容忽视。为满足特殊患者的长期治疗需求,口服剂型的开发十分重要。为克服多肽药物口服剂型的种种障碍,各企业进行了各种尝试,包括分子本身的结构修饰与环化、优化药物载体、添加吸收促进剂、使用药械组合等。环孢素和司美格鲁肽的成功证实了多肽口服的可行性。
总体而言,口服多肽药物的开发一直是充满挑战和前景的领域。虽然目前口服多肽制剂在利用率、服用便捷性等方面还存在很大的提升空间。但我们仍然期待通过汲取过往经验并采用新技术,这类药物的开发必将取得突破。在后续文章中,我们将继续探讨现阶段口服多肽制剂新的开发技术。
科生景肽:多肽药物发现与递送的引领者
合肥科生景肽生物科技有限公司成立于2018年,目前已经打造了全球领先的以肽为核心的生命分子发现、合成生产、结构优化、递送平台,主要瞄准肽发现及靶向递送,专注于为各大制药企业、生物技术公司、科研单位提供一站式的定制化研发服务。
公司独有的KPDS™平台(KS-V Peptide Discovery Services Platform)是国际领先的的多肽药物发现平台,我们致力于创新药物的高效和精准开发,以科生景肽专有KPDS技术为核心,提供一站式,定制化的多肽发现服务,以灵活的产品形式和服务模式助力广大客户各类药物发现项目的快速推进和应用探究,包括但并不限于疾病诊断及保健功能产品、多肽药物、核素偶联药物(RDC)、基于小分子的肽药物偶联物(PDC)和多功能肽偶联物等。